 燃料電池の基礎知識
燃料電池の基礎知識
1.燃料電池とは:
燃料としての水素と酸素から水を生成する反応において、
水素の電子の電気エネルギーをとりだす発電装置。
2.乾電池との違い:
乾電池は電池本体に電気エネルギーを蓄えている
電気の貯水槽であるのに対して、燃料電池は外部からの
燃料供給により電気エネルギーを作りだす電気の生産工場(発電装置)。
3.燃料電池の将来性:
燃料電池から排出される物質はその大部分が水であり、
環境にもやさしく、将来、次世代新エネルギー源の柱になる
ともいわれています。
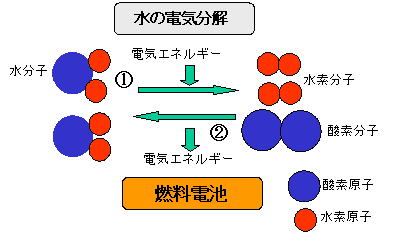
【図1】
① 水に電気を流すと水素と酸素に分かれます。これが水の電気分解です。
② 燃料電池はこの逆の反応です。水素と酸素から水を作る際に電気エネルギーを取り出す装置が燃料電池です。
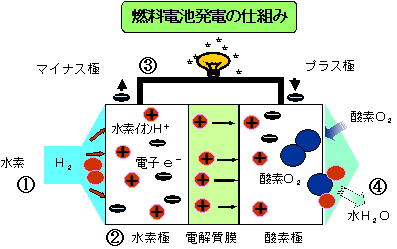
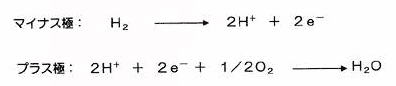
【図2】
① 図左側から水素が水素極に流れてきます。
② 水素は電解質膜と水素極の間に存在する触媒の働きでプロトン(水素イオンH+)と電子(e-)に分かれます。
分かれたプロトン(H+)は電解質膜中を通過できますが、電子(e-)は通り抜けることが出来ません。
電子(e-)は水素極に蓄積されて行きます。
③ 水素極と酸素極に電線と負荷対象物をつなぐと、電子(e-)は蓄積されている水素側から酸素側に
流れていきます。このときに負荷対象物を稼動させる事が出来ます。(電気が流れた事になります)
④ 図右の酸素極では電解質膜を通過してきたプロトン(H+)と酸素極に供給されている酸素と水素側
から移動してきた電子(e-)とが化学反応し,水が生成されることになります。
全体の反応は水素と酸素から水ができることになります。